GCGR激动剂被二拒
2024-10-15
来源: drugdu
 430
430
原创 时光 生物制药小编 2024年10月14日 09:20 上海
减肥药概念股Zealand公司再次受挫,推出的用以治疗儿童先天性高胰岛素血症(CHI)的上市申请的新药Dasiglucagon再次遭到了FDA拒绝。
去年12月,因为发现第三方合同制造工厂缺陷,Dasiglucagon首次被FDA拒之门外。
Zealand指出,Dasiglucagon二次被拒主要原因在于,FDA对第三方生产工厂的复检没能完成,导致审批进程搁置,FDA并没有提出对dasiglucagon有效性或安全性的担忧。
Dasiglucagon是一种胰高血糖素受体(GCGR)激动剂,其作用是使肝脏将储存的糖原释放到血液中。
低血糖是糖尿病最常见的急性并发症之一,患者在有能力持续监测血糖的情况下也并不能完全预防严重低血糖事件。
与未发生严重低血糖的患者相比,发生严重低血糖的2型糖尿病患者心力衰竭以及动脉粥样硬化性心血管疾病的风险增加,全因死亡率和短暂性脑缺血发作风险均增加。此外,反复发作的低血糖可能加剧患者的脑缺血性损伤,影响患者免疫反应等。
2021年,Dasiglucagon获得FDA批准上市,用于治疗6岁及以上糖尿病患者的严重低血糖。2022年6月,Zealand与诺和诺德就Dasiglucagon全球许可和开发协议,总交易额为4575万美元,Dasiglucagon将该药的全球商业化交给了后者负责。
Zealand成立于1998年,公司与另一家诺和诺德在地理位置上只隔几英里,Zealand的 CEO在内的多位管理层也曾有在诺和诺德工作的经历。
2010年和2017年,Zealand分别在在丹麦哥本哈根交易所上市以及美国纳斯达克交易所和上市。
Zealand最初也是做降糖,Zealand推出的首个上市产品——利西拉来就是一款GLP-1受体激动剂,不过在2003年便授权给了赛诺菲。
近年来因为减肥药的大火,加上之后推出的Dasiglucagon销售业绩表现不佳,Zealand也转变了研发方向,专注于减重药的开发。
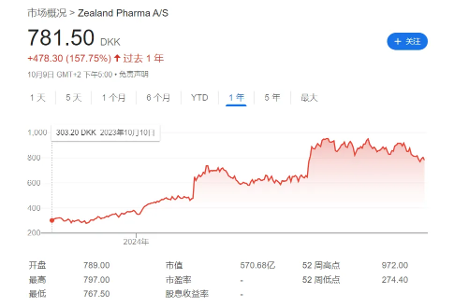
可以说,这个战略转变对于Zealand的起死回生十分关键,受到减重药利好临床数据的拉动,公司近一年股价上涨了158%。
 Zealand围绕减重布局了多款管线,其中最快的Survodutide已经推进到Ⅲ期临床阶段,Survodutide是一种GCGR/GLP-1R双靶点激动剂,与勃林格殷格合作开发,适应症包括减重和MASH。
Zealand围绕减重布局了多款管线,其中最快的Survodutide已经推进到Ⅲ期临床阶段,Survodutide是一种GCGR/GLP-1R双靶点激动剂,与勃林格殷格合作开发,适应症包括减重和MASH。
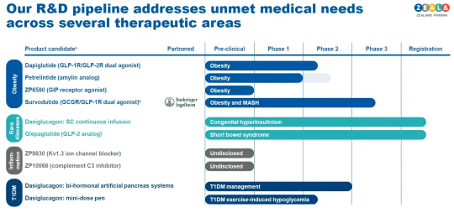 Zealand还开发了全球首款GLP-1/GLP-2双重激动剂Dapiglutide,目前已经推进到临床Ⅱ期阶段。
Zealand还开发了全球首款GLP-1/GLP-2双重激动剂Dapiglutide,目前已经推进到临床Ⅱ期阶段。
上个月,Zealand公布了dapiglutide用于减重的II期临床数据,13周时,Dapiglutide组最高减重6.2%,而安慰剂组体重增加了2.1%。
还有两款减重管线——一种胰淀素类似物Petrelintide、以及一款GIP受体激动剂ZP6590。
因为Dasiglucagon卖的不行,本来Zealand也是缺钱的,去年公司还与一家欧洲投资银行签署了一项9000万欧元的贷款融资协议。
今年公司财务状况明显好转,在股票市场的正向表现令公司今年6月通过增发募资了70亿丹麦克朗(约合10亿美元),解下了资金燃眉之急。
去年底,Zealand还向FDA递交另外一款新药的上市申请——glepaglutide,一种长效胰高血糖素样肽-2(GLP-2)类似物,用于治疗依赖肠外营养支持的成人短肠综合征患者。
相关News
- MNC再落一子,禽用疫苗获批上市 2026-05-29
- 295万研发投入,斩获24亿便秘大品种 2026-05-29
- 诺诚健华奥布替尼在澳大利亚获批上市 2026-05-29
- 赛生药业新型抗生素注射用盐酸替拉凡星在中国上市 2026-05-29
- 全球首个:艾伯维CD123 ADC获批上市 2026-05-29





