EGFR 突变 NSCLC ORR 达 80%!智康弘义 CDH3 ADC 公布最新临床结果
2024-09-25
来源: drugdu
 339
339
Insight数据库 2024年09月24日 14:32 浙江
9 月 14 日,智康弘义在 2024 年 ESMO 年会上公布了全球独家开发的抗体偶联药物 BC3195(CDH3 ADC)在 I 期临床试验中针对晚期实体瘤的安全性和有效性的最新临床数据(NCT05957471)。对携带 EGFR 突变的患者 ORR 达到 80%。

BC3195 采用与 CDH3 蛋白具有较高亲和力并展现出良好内吞活性的抗体,同时采用经临床验证、具有「旁观者效应」的连接子和有效载荷 vc-MMA。
此次发布的数据显示,BC3195 具有可控的安全性和良好的 PK 特征。BC3195 在 NSCLC 患者中显示出显著的抗肿瘤活性,其总体缓解率(ORR)达到 36.4%,尤其是对携带 EGFR 突变的患者 ORR 达到 80%。
数据截止日期为 2024 年 8 月 10 日,该 I 期临床研究共入组了 34 例患者,均为经历多线治疗的晚期患者。其中 0.3、0.6、1.2 和 1.8 mg/kg Q3W 剂量组四个剂量组各入组 3 例患者,2.4 mg/kg Q3W 剂量组入组 21 例患者,1.2 mg/kg QW 剂量组入组 1 例患者。
在 30 例可评估肿瘤反应的患者中,1.8 mg/kg Q3W 及以下剂量组没有报告完全缓解(CR)或部分缓解(PR)
在 2.4 mg/kg Q3W 剂量组中,5 例患者最佳反应为部分缓解,且均获确认(cPR),其中 4 例为非小细胞肺癌患者、1 例为乳腺癌患者。
在接受 2.4 mg/kg 治疗的 11 例非小细胞肺癌(NSCLC)患者中,10 例患者的肿瘤体积缩小,其中 4 例患者确认为部分缓解(cPR),6 例患者的最佳反应为疾病稳定(SD),ORR 和 DCR 分别为 36.4% 和 90.9%;在 5 例携带 EGFR 突变的 NSCLC 患者中,有 4 例确认的 PR(cPR),ORR 达到 80%,其中一名获得 cPR 的患者曾经过 5 线治疗,PR 缓解时间已持续 20 周。
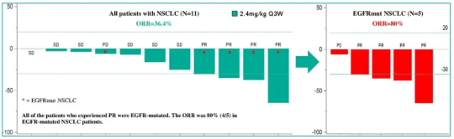 BC3195在 2.4 mg/kg Q3W剂量水平上
BC3195在 2.4 mg/kg Q3W剂量水平上
针对NSCLC的最佳疗效
安全性方面,34 例患者中,仅在 2.4 mg/kg Q3W 剂量组中发生一起剂量限制性毒性(DLT)事件,为 3 级咽炎。主要不良事件(AEs)为皮疹、口腔炎及肝功能检测异常,多数皮疹和口腔炎不良事件发生在第一个给药周期,且安全性可控
14 例患者(41.2%)发生了≥3 级的治疗相关不良事件(TRAEs),其中超过 2 例患者发生了口腔炎(23.5%)、中性粒细胞计数减少(8.8%)和皮疹(8.8%)。
BC3195 目前正在中美同步进行开展 I 期剂量优化和剂量扩展研究。
相关News
- MNC再落一子,禽用疫苗获批上市 2026-05-29
- 295万研发投入,斩获24亿便秘大品种 2026-05-29
- 诺诚健华奥布替尼在澳大利亚获批上市 2026-05-29
- 赛生药业新型抗生素注射用盐酸替拉凡星在中国上市 2026-05-29
- 全球首个:艾伯维CD123 ADC获批上市 2026-05-29





