FDA 批准 LEO Pharma 的 Adbry 扩大适应症用于患有特应性皮炎的儿科患者
2023-12-25
来源: drugdu
 629
629
制药执行编辑人员
Adbry(tralokinumab-ldrm)的适应症扩大到包括 12 至 17 岁患有中度至重度特应性皮炎的患者,这些患者的疾病不能通过局部处方疗法得到充分控制,或者医生不建议通过这些疗法控制疾病。
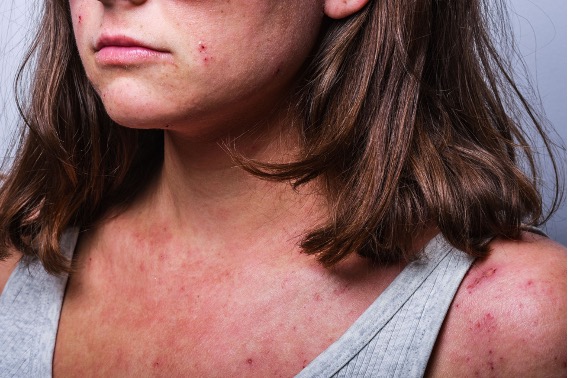
FDA 已批准 LEO Pharma 的 Adbry (tralokinumab-ldrm) 的扩大适应症,用于治疗 12 至 17 岁患有中重度特应性皮炎 (AD) 的患者,这些患者的疾病无法通过局部处方疗法得到充分控制,或者这些疗法不建议用来治疗那些患有中度至重度特应性皮炎 (AD) 的患者。 Adbry 是一种人免疫球蛋白 G4 单克隆抗体,可特异性结合人白细胞介素 (IL)-13,并抑制其与 IL-13 受体 α1 和 α2 亚基的相互作用。 Adbry 是 FDA 批准用于该适应症的第一个也是唯一一个生物制剂。
LEO Pharma执行副总裁兼总裁布莱恩·希尔伯丁克 (Brian Hilberdink) 在北美地区的一份新闻稿中表示:“这是我们为那些最需要帮助的人带来根本性改变的一个重要里程碑。这个关键患者群体现在可以获得急需的额外治疗选择来控制他们的特应性皮炎。” “我们很高兴能够为美国的成人和儿童患者提供 Adbry,一种高度针对性的治疗方法。 这种使人衰弱的疾病会对儿科患者产生特别强烈的影响,他们经常因为自己的病情而感到被社会孤立。 我们自豪于迄今为止所取得的进展,也将继续努力满足更多患者群体中未满足的需求。”
在临床试验中,该药物显著改善了 12 至 17 岁中重度 AD 患者的瘙痒、睡眠干扰、焦虑、抑郁和整体生活质量。对于该患者组,扩大的适应症是初始负荷剂量为每两周服用300毫克,随后每两周服用 150 毫克。
FDA 对 Adbry 扩大适应症的批准是基于 III 期 ECZTRA 6 试验的数据。 研究人员在 289 名年龄为 12-17 岁、患有中度至重度 AD 且适合全身治疗的患者中评估了该药物的疗效和安全性。 在参加该试验的患者中,有 98 名患者接受了初始剂量的300毫克 Adbry ,随后每隔一周服用 150 毫克,直至第 16 周。
研究表明,服用 Adbry 的患者中有 21% 研究者总体评估 (IGA) 得分为 0 或 1,而服用安慰剂的患者为 4%。 该试验还发现,与服用安慰剂的 6% 患者相比,服用 Adbry 的患者中有 29% 的湿疹面积和严重程度指数评分 (EASI-75) 改善了至少 75%。
此外,服用 Adbry 的患者中,有 23% 的青少年最严重瘙痒症数值评定量表下降了至少 4 分,而安慰剂组的这一比例为 3%,并且与服用安慰剂的患者相比,服用 Adbry 的患者中有更大比例的 EASI-90 至少改善了 90%。
ECZTRA 6 国际协调研究员、芝加哥西北大学范伯格医学院皮肤科系主任艾米·帕勒(Amy Paller)医学博士在一份新闻稿中表示:“我们知道与中度至重度特应性皮炎相关的症状可能会对儿科患者产生影响,这就是为什么拥有在减少瘙痒和皮肤清洁方面,已证明有效的治疗选择如此重要。” “提供这一证据的临床试验结果对于临床医生评估儿科患者治疗方案的安全性和有效性来说非常宝贵。”
在安全性方面,该药物的概况与成人特应性皮炎临床试验中报告的情况相当。成人最常见的不良事件是上呼吸道感染、结膜炎、注射部位反应和嗜酸性粒细胞增多。
国家湿疹协会主席兼首席执行官朱莉·布洛克 (Julie Block) 在一份新闻稿中表示:“Adbry 的批准用于患有中度至重度特应性皮炎的儿科患者,扩大了这种疾病的患者的治疗选择,而这些患者历来的选择有限。” “特应性皮炎治疗领域的此类进展为寻求合适的长期治疗选择的儿科患者提供了急需的希望。
责编: editor相关News
- 喜报!美阿沙坦钾片获批 2026-05-26
- 海正药业前列腺癌治疗药物获批上市 2026-05-26
- 华东医药首个精准靶向EGFR外显子21(L858R)创新药马来酸美凡厄替尼迈瑞东®开出全国首张处方 2026-05-26
- 普洛药业琥珀酸美托洛尔缓释片新增25mg规格获美国FDA批准 2026-05-26
- 日本制药巨头,被判赔170亿 2026-05-26





