突破心脏石化“不可逆”-ATTR-CM治疗从防守转向反攻
2026-04-10
来源: drugdu
 135
135
转甲状腺素蛋白淀粉样变心肌病(ATTR-CM)的故事,要从一个蛋白质的结构失稳讲起。TTR蛋白正常情况下以四聚体的形式在血液中运输甲状腺素和维生素A,结构稳定,各司其职。但在衰老或特定基因突变的影响下,四聚体会解离为单体,单体发生错误折叠,进而聚集成不可降解的淀粉样纤维。这些纤维一旦沉积在心肌间质中,心壁就会增厚、变硬,导致顺应性下降,舒张功能逐步丧失,最终走向心力衰竭。
过去很长时间里,临床对这类疾病的态度基本上是“守”,用药物稳住蛋白结构,减缓沉积速度,尽量把病程拖长一些。至于已经嵌入心肌的那些纤维,大家默认没有办法。但最近几年,局面开始松动。单克隆抗体清除剂在临床试验中拿出了逆转心肌损伤的早期证据,基因编辑技术则想从基因组层面一次性解决问题。治疗的底层逻辑正在从“延缓恶化”转向“主动清除”。
本文沿着三代治疗策略的技术演进,梳理各自的临床数据、产业格局与尚未回答的问题。
致病机理:四聚体解体与纤维沉积
ATTR-CM过去一直被归为罕见病。但近年来随着筛查手段的进步,这个判断正在被修正。在射血分数保留的心衰(HFpEF)患者中,ATTR-CM的检出率大约在20%左右。换句话说,相当一部分患者可能长期被笼统地诊断为“舒张性心衰”,真正的病因一直没被揪出来。
致病过程本身并不难理解:TTR四聚体在老化或突变驱动下解离为单体,单体错误折叠,折叠异常的单体聚集成淀粉样纤维,纤维在心肌间隙持续堆积,心室壁增厚变硬,舒张功能进行性丧失。这条通路上的每一个环节,理论上都可以是药物干预的靶点。实际“走通了”哪些,“没走通”的卡在哪里,下面将逐一剖析导致。
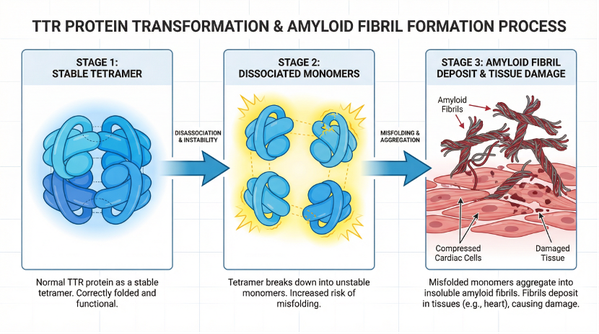 图1:TTR蛋白从稳定的四聚体解离为单体,最终错误折叠并聚集成淀粉样纤维,导致心肌细胞受压迫的过程
图1:TTR蛋白从稳定的四聚体解离为单体,最终错误折叠并聚集成淀粉样纤维,导致心肌细胞受压迫的过程
数据来源:公开数据整理
一个容易被错过的早期信号
临床研究发现一个有趣的现象:不少ATTR-CM患者在出现心脏症状之前5到10年,会先出现腕管综合征或肱二头肌肌腱断裂。道理不复杂——异常蛋白倾向于在机械应力较大的组织率先聚集,韧带和肌腱首当其冲。这个发现的临床价值在于它提供了一个筛查的时间窗口。问题是,腕管综合征归骨科管,心肌病归心内科,两边的信息在大多数医院里并不互通。如果能在骨科端建立对高危人群的转诊意识,相当于把诊断窗口前移了五到十年。
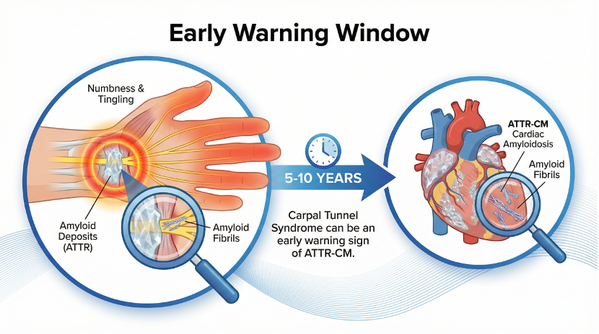 图2:腕管综合征作为ATTR-CM早期预警信号的时间线与病理机制
图2:腕管综合征作为ATTR-CM早期预警信号的时间线与病理机制
数据来源:公开数据整理
三代治疗策略
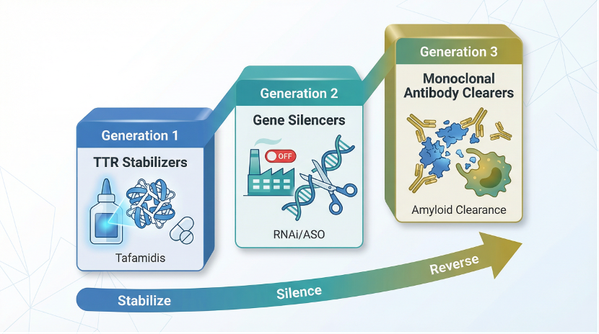 图3:ATTR-CM 治疗方案从稳定剂、基因沉默到单克隆抗体清除的三代演进
图3:ATTR-CM 治疗方案从稳定剂、基因沉默到单克隆抗体清除的三代演进
数据来源:公开数据整理
针对ATTR-CM的药物开发,沿着三个方向依次展开。下表是一个快速对照:
第一代防线:TTR稳定剂
稳定剂的逻辑很直接:既然问题始于四聚体解离,那就用小分子把四聚体锁住,不让它散架。
Tafamidis是这个类别的开山之作,也是全球首个获批用于ATTR-CM的疾病修正药物。临床数据显示TTR稳定效率约70%–80%,治疗组全因死亡率较安慰剂降低36%。辉瑞2010年收购FoldRx获得该药,如今Vyndaqel系列已是其罕见病板块的绝对支柱:2024年全球销售额54.5亿美元,同比增长65%;2025年Q2单季16.2亿。Acoramidis是后来者,由Eidos Therapeutics开发。它的结合亲和力更强,机制上模拟T119M保护性突变来强化氢键与盐桥相互作用,TTR稳定率接近100%。
但不管是Tafamidis还是Acoramidis,天花板是一样的:它们只管“增量”问题——阻止新的纤维生成。至于已经嵌入心肌间质里的存量纤维,稳定剂“够不着”。
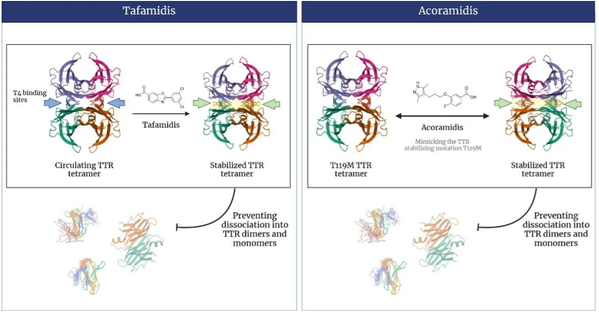 图4:稳定剂药物Tafamidis和Acoramidis的作用机制
图4:稳定剂药物Tafamidis和Acoramidis的作用机制
图片来源:医脉通心血管
第二代:TTR沉默剂在源头关掉生产线
稳定剂锁住了现有的四聚体,但肝脏还在源源不断地合成新的TTR蛋白。沉默剂的想法更激进:既然管不住下游,就直接去上游把生产线关掉。TTR几乎完全由肝脏合成,且由单一基因编码,天然适合siRNA和ASO技术的靶向——靶点明确、器官集中、递送路径成熟。
这条赛道目前Alnylam一家独大。Patisiran(Onpattro)是全球首款获批siRNA药物(2018年,适应症为ATTR多发性神经病),但并未拿到ATTR-CM适应症。真正在心肌病领域打开局面的是其迭代产品Vutrisiran(Amvuttra),采用GalNAc偶联技术,每三个月皮下注射一次,TTR蛋白水平降幅约88%,目前是唯一获批用于ATTR-CM的沉默剂。上市后增长很猛:2024年上半年销售额4.25亿美元,同比增长82%。
沉默剂的局限和稳定剂本质上是同一个:它关掉了水龙头,但地板上已经积的水不会自己蒸发。因此,对疾病较晚期的患者来说,心肌中存量纤维的负担才是核心矛盾,单靠阻断新增远远不够。
第三代:TTR清除剂触及存量纤维
前两代药物有一个共同的局限:不管是锁住四聚体还是关掉TTR的合成,它们都只作用于“增量”。对已经嵌入心肌间质的存量纤维,束手无策。第三代清除剂要解决的,正是这个问题。
技术上的关键在于靶向精度。TTR蛋白在正常四聚体状态下,内部有一段氨基酸序列被紧密包裹,从表面无法识别。但当四聚体解离、单体错误折叠后,这段序列翻转暴露出来,形成所谓的“隐蔽表位(Cryptic Epitope)”。清除剂抗体专门识别这个仅在异常构象上才出现的标记——这意味着循环血液中正常工作的TTR四聚体不会被误伤。抗体与沉积纤维结合后,通过Fc段招募巨噬细胞至沉积部位,由后者完成对纤维的吞噬和降解。
目前进展最快的两个分子是AstraZeneca/Alexion的Cliramitug(NI006,最初由Neurimmune开发)和Novo Nordisk的Coramitug(NNC6019,来自Prothena)。两者都已进入III期临床,具体数据在产业格局部分展开。
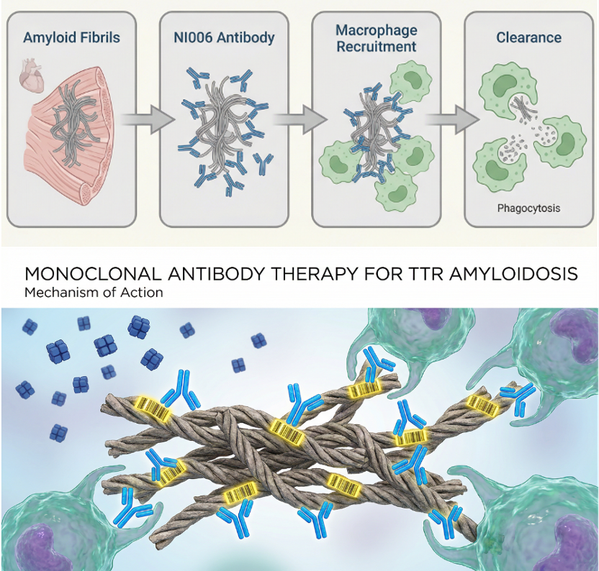 图5:单克隆抗体精准锁定淀粉样纤维上的特定序列,引导巨噬细胞进行清理,而不影响正常的TTR四聚体
图5:单克隆抗体精准锁定淀粉样纤维上的特定序列,引导巨噬细胞进行清理,而不影响正常的TTR四聚体
数据来源:公开数据整理
安全剂量设计:为什么不能简单爬坡
清除剂有一个绕不开的安全性问题。大量巨噬细胞被招募到心肌沉积部位,本质上就是在一颗已经功能受损的心脏里制造局部炎症。如果炎症反应失控,对这类患者来说后果可能是致命的。所以常规的“从低剂量开始往上爬”在这个场景里风险很大:爬坡本身就是在赌。
Cliramitug团队选择了一条更稳妥的路:在进入人体试验之前,先建立跨物种的机制性PK/PD模型。具体做法是整合大鼠药代动力学数据和人类心脏活检组织的体外实验结果,把剂量方案在计算层面先推演到位。模型给出的关键参数是:起始剂量0.3mg/kg,靶点占有率控制在18%以下;有效剂量窗口10–60mg/kg,预测4到10个月内可显著减少心肌淀粉样沉积。
后续的临床数据证实了这些预测。这套“先建模、后进人”的策略,在安全窗口极窄的清除剂领域可能会成为一个方法论模板。
基因编辑:一次给药的可能性
沉默剂需要持续给药才能维持TTR的低水平:Amvuttra三个月一次,Eplontersen一个月一次。基因编辑想做的事情更彻底:直接在基因组层面敲除或修改TTR基因,一次给药,长期受益
基因编辑对晚期患者的价值尤其明显。这些患者用了稳定剂之后,进展虽然放慢了,但心功能仍然在持续走下坡。如果基因编辑能永久关闭TTR来源,再联合清除剂处理存量沉积,“断源+清库”的组合在理论上是最完整的干预方案。当然,从理论到落地之间还隔着长期安全性和脱靶效应这两道关,目前都还没有确定性的答案。
产业格局:三条赛道上的卡位
稳定剂赛道目前是辉瑞的地盘。Tafamidis(Vyndaqel/Vyndamax)2024年全球销售额54.5亿美元,同比增长65%。但美国专利2028年到期,仿制药的压力已经在倒计时了。
沉默剂赛道以Alnylam为核心。Amvuttra获批后放量很快,上市三个季度就拿下了35%的新药市场份额。Eplontersen(Ionis/AstraZeneca)的III期正在赛跑。
清除剂赛道的格局最有看头。诺和诺德从Prothena引进Coramitug,潜在里程碑付款总额12亿美元,III期CLEOPATTRA试验正在推进(约1280人,预计2029年完成)。另一边,阿斯利康/Alexion的Cliramitug III期DepleTTR-CM于2024年1月启动,计划入组1000至1181人,预计2027—2028年完成。两家几乎同时在同一个赛道砸下重注,谁先拿出关键数据,谁就定义下一代治疗标准。
随着核素显像等无创诊断手段的普及,被识别出的ATTR-CM患者基数还在持续扩大。全球ATTR淀粉样变治疗市场预计2031年达到142.8亿美元。
做心血管方向的药物研发,第一课就是学会敬畏心肌组织的脆弱。心肌组织是药物设计的硬约束条件之一。它对毒性极其敏感,再生能力几乎为零。一个分子的亲和力再高,只要在hERG通道上有毒性信号,项目基本就推进不下去了。ATTR-CM的治疗史,某种意义上就是这堂课的三次考试。第一次,我们学会了用小分子把正在散架的蛋白质粘回去,阻止新的伤害发生。第二次,我们直接去肝脏关掉了生产故障蛋白的那条线。第三次我们试着让抗体带着巨噬细胞,去清理已经嵌入心肌里的那些纤维。站在现在的起点,可以回顾到的是十年前业内还不曾认为第三步是可能的。
但科学上的“可能”和临床上的“可及”之间,隔着一张价目表。Tafamidis在美国的年度采购成本约26.8万美元。Vutrisiran和Eplontersen超过50万,这还只是单药。如果未来的最优方案是沉默剂加清除剂、甚至再叠一次基因编辑,总费用会是什么量级,目前没有人愿意算这笔账。做药的人习惯讨论分子的亲和力、选择性、PK参数。但一个药最终能否惠及大众,往往无法直接取决于Kd值,而取决于患者的诸多客观因素。这大抵是无法使用教学理论,但也是每个新药人会需要面对的问题。
https://news.yaozh.com/archive/47737.html
责编: editor相关News
- 喜报!美阿沙坦钾片获批 2026-05-26
- 海正药业前列腺癌治疗药物获批上市 2026-05-26
- 华东医药首个精准靶向EGFR外显子21(L858R)创新药马来酸美凡厄替尼迈瑞东®开出全国首张处方 2026-05-26
- 普洛药业琥珀酸美托洛尔缓释片新增25mg规格获美国FDA批准 2026-05-26
- 日本制药巨头,被判赔170亿 2026-05-26





