全球首个!安进/阿斯利康重磅炸弹药物在中国获批上市
2026-03-31
来源: drugdu
 184
184


3 月 27 日,NMPA 官网显示,阿斯利康和安进联合递交的 TSLP 单抗特泽利尤单抗注射液获批上市。本次该药获批 2 个适应症,分别是哮喘(受理号:JXSS2400102/3)和慢性鼻窦炎伴鼻息肉病(受理号:JXSS2500019/20)。 
![]()
截图来源:NMPA 官网特泽利尤单抗由阿斯利康与安进合作开发,是一种同类首创的人类单克隆抗体,可抑制 TSLP 的作用。TSLP 是一种关键的上皮细胞因子,位于多个炎症级联的顶端,与严重哮喘和其他炎症疾病相关的过敏性、嗜酸性和其他类型内皮炎症息息相关。2021 年该药首次获 FDA 批准上市,用于患有严重哮喘的成人和 12 岁及以上的儿童患者的附加维持治疗,2022 年该药先后在欧盟和日本获批。2025 年 10 月,该药新增适应症成功,在美国获批用于治疗 12 岁及以上成人和儿童慢性鼻窦炎伴鼻息肉(CRSwNP)控制不佳的维持治疗。 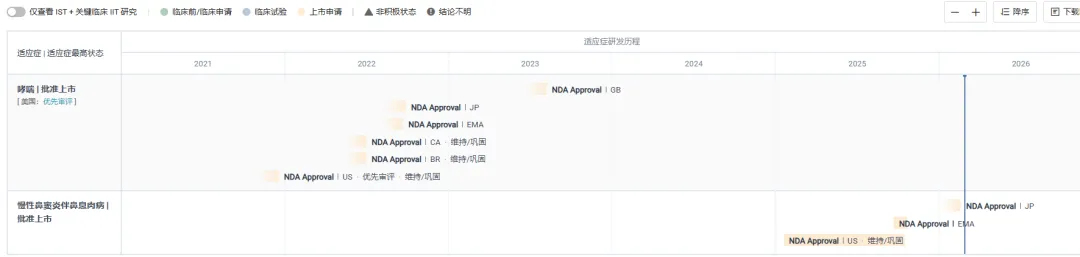
在国内,该药已启动针对哮喘、嗜酸性粒细胞性食管炎、慢性鼻窦炎伴鼻息肉病、慢性阻塞性肺疾病的 III 期临床。
哮喘
一项关于哮喘的 DESTINATION 临床试验已经完成。这是一项区域性、多中心、随机、双盲、安慰剂对照、平行组、III 期研究,旨在评价特泽利尤单抗在重度哮喘控制不佳的成年受试者中的有效性和安全性。
在 2025 年美国过敏、哮喘和免疫学会年会(AAAAI)上公布的临床结果显示,与安慰剂相比,特泽利尤单抗在 52 周内显著降低患者哮喘急性发作率(AAER)达 74%。
在次要终点方面,与安慰剂相比,特泽利尤单抗在 52 周内显著改善患者肺功能,FEV1 改善达 250 ml,并显著改善患者哮喘症状控制及生活质量(根据 ACQ-6、AQLQ[S]+12 和 ASD 评估,治疗 52 周后,上述评分较基线均有显著改善)。
慢性鼻窦炎伴鼻息肉病
III 期 WAYPOINT 临床研究的阳性结果表明,与安慰剂相比,特泽利尤单抗显著减轻了慢性鼻窦炎伴鼻息肉患者的鼻息肉严重程度,减少患者后续鼻息肉手术的需求及系统性糖皮质激素使用的需求。相关数据发表于《新英格兰医学杂志》,并在 2025 年 AAAAI 大会上以最新突破性研究口头报告形式发布。
数据显示,使用特泽利尤单抗治疗显著降低了通过共同主要终点评估的鼻息肉严重程度:与使用安慰剂相比,治疗第 52 周时,鼻息肉评分(NPS)降低了 2.065 分,患者自我报告鼻塞症状评分(NCS)降低了 1.028 分 。NPS 的改善最早见于第 4 周,NCS 的改善最早见于第 2 周(分别为第一次治疗后评估),且疗效持续至第 52 周 。
在研究总体人群中,所有关键次要终点均显示出统计学意义及临床意义的改善。尤为重要的是,与安慰剂组相比,特泽利尤单抗显著减少了患者后续鼻息肉手术的需求(降幅达 98%)和系统性糖皮质激素使用的需求(降幅达 88%)。
Insight 视角
Insight 数据库显示,特泽利尤单抗是目前全球唯一一款获批上市的 TSLP 单抗,2025 年大卖近 20 亿美元,首次上榜全球药品销售额 TOP100 榜单。除此之外,有 6 款已进入临床 III 期,分别来自博奥信/正大天晴(Bosakitug)、恒瑞/GSK(GSK5784283)、康诺亚/石药(CM326)、荃信生物(JKN24011)等,其中齐鲁制药 QL2302 是一款特泽利尤单抗生物类似药。

免责声明:
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部。
https://mp.weixin.qq.com/s/JYs0t7J2oB-SiYu1QJobXw
责编: editor相关News
- 礼来大药,首仿刚批,第三家申报上市! 2026-05-15
- 152亿美元大单,一哥炸场! 2026-05-15
- 重磅!青峰医药斩获双首仿,百亿市场风云再起 2026-05-15
- 吉利德HIV新药“超预期” 2026-05-15
- 半年三捷!甘李药业再下一城:赖脯胰岛素获欧盟批准,国产胰岛素首破欧洲原研垄断 2026-05-15





