礼来,再下一城!来瑞奇珠单抗在华申报上市
2026-03-05
来源: drugdu
 269
269
 3月3日,中国国家药监局药品审评中心(CDE)官网公示显示,礼来(Eli Lilly and Company)申报的3.1类新药来瑞奇珠单抗注射液上市申请获得受理。
3月3日,中国国家药监局药品审评中心(CDE)官网公示显示,礼来(Eli Lilly and Company)申报的3.1类新药来瑞奇珠单抗注射液上市申请获得受理。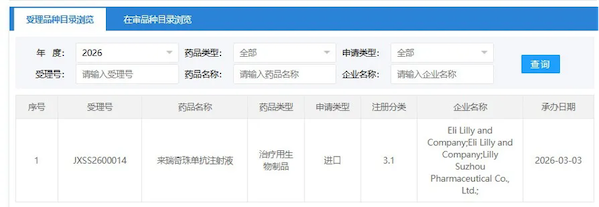 来瑞奇珠单抗(Lebrikizumab)是一种白细胞介素-13(IL-13)抑制剂,能够以高结合亲和力和缓慢解离速率选择性地靶向并中和IL-13。来瑞奇珠单抗与IL-13细胞因子结合的位置与IL-13Rα1/IL-4Rα异源二聚体中IL-4Rα亚基的结合位点重叠,从而阻止该受体复合物的形成并抑制IL-13信号传导。IL-13是特应性皮炎的一种主要细胞因子,驱动皮肤中的2型炎症循环,导致皮肤屏障功能障碍、瘙痒、皮肤增厚和感染。来瑞奇珠单抗的开发经过了一系列曲折的过程。该药最早由罗氏原研,2008 年就开启了首个临床试验,但在首发适应症哮喘上并不顺利,于 2016 年在两项 III 期临床上一胜一败。2017 年 8 月,罗氏将该药授权转让给 Dermira 公司;2019 年,Dermira 公司将欧洲地区的选择权转让给 Almirall 公司;2020 年,礼来收购 Dermira 公司,囊获这一产品。2023年11月,来瑞奇珠单抗首次在欧洲获批上市,随后于2024年9月在美国获批上市,适用于治疗患有中度至重度特应性皮炎(AD)的12岁及以上青少年和成人患者。据礼来2025年报,来瑞奇珠单抗全球销售额约为4.08亿美元。礼来拥有在美国和除欧洲以外的全球其他地区开发和商业化来瑞奇珠单抗的独家权利。来瑞奇珠单抗的批准主要基于 ADvocate 1、ADvocate 2 和 ADhere 研究的结果,这些研究主要评估入组患者在 16 周时的皮肤症状清除情况。在ADvocate 1研究中,治疗第16周,来瑞奇珠单抗组和安慰剂组达到研究者总体评估评分为0或1(IGA 0/1)且较基线至少下降2分的受试者比例分别为43.1%和12.7%(P<0.001),达到湿疹面积和严重程度指数至少改善75%(EASI-75)的受试者比例分别为58.8%和16.2%(P<0.001)。在ADvocate 2研究中,治疗第16周,来瑞奇珠单抗组和安慰剂组达到IGA 0/1且较基线至少下降2分的受试者比例分别为33.2%和10.8%(P<0.001),达到EASI-75的受试者比例分别为52.1%和18.1%(P<0.001)。结果显示,经过 16 周的治疗,来瑞奇珠单抗组有 38% 的患者皮肤症状清除或几乎清除(IGA 0 或 1),而安慰剂组为 12%。在症状清除或几乎清除的患者中每月一次用药,77% 的患者维持缓解达到一年。在国内,礼来于 2024 年登记了一项多中心、随机、双盲、安慰剂对照、III 期试验,旨在中至重度特应性皮炎受试者中评价来瑞奇珠单抗联合/不联合外用皮质类固醇治疗时的有效性和安全性。研究的主要终点是第 16 周达到 EASI-75 的受试者比例。具体研究结果尚未披露。目前全球仅有两款IL-13单抗获批上市,即Tralokinumab(Leo Pharm)和来瑞奇珠单抗(礼来)。
来瑞奇珠单抗(Lebrikizumab)是一种白细胞介素-13(IL-13)抑制剂,能够以高结合亲和力和缓慢解离速率选择性地靶向并中和IL-13。来瑞奇珠单抗与IL-13细胞因子结合的位置与IL-13Rα1/IL-4Rα异源二聚体中IL-4Rα亚基的结合位点重叠,从而阻止该受体复合物的形成并抑制IL-13信号传导。IL-13是特应性皮炎的一种主要细胞因子,驱动皮肤中的2型炎症循环,导致皮肤屏障功能障碍、瘙痒、皮肤增厚和感染。来瑞奇珠单抗的开发经过了一系列曲折的过程。该药最早由罗氏原研,2008 年就开启了首个临床试验,但在首发适应症哮喘上并不顺利,于 2016 年在两项 III 期临床上一胜一败。2017 年 8 月,罗氏将该药授权转让给 Dermira 公司;2019 年,Dermira 公司将欧洲地区的选择权转让给 Almirall 公司;2020 年,礼来收购 Dermira 公司,囊获这一产品。2023年11月,来瑞奇珠单抗首次在欧洲获批上市,随后于2024年9月在美国获批上市,适用于治疗患有中度至重度特应性皮炎(AD)的12岁及以上青少年和成人患者。据礼来2025年报,来瑞奇珠单抗全球销售额约为4.08亿美元。礼来拥有在美国和除欧洲以外的全球其他地区开发和商业化来瑞奇珠单抗的独家权利。来瑞奇珠单抗的批准主要基于 ADvocate 1、ADvocate 2 和 ADhere 研究的结果,这些研究主要评估入组患者在 16 周时的皮肤症状清除情况。在ADvocate 1研究中,治疗第16周,来瑞奇珠单抗组和安慰剂组达到研究者总体评估评分为0或1(IGA 0/1)且较基线至少下降2分的受试者比例分别为43.1%和12.7%(P<0.001),达到湿疹面积和严重程度指数至少改善75%(EASI-75)的受试者比例分别为58.8%和16.2%(P<0.001)。在ADvocate 2研究中,治疗第16周,来瑞奇珠单抗组和安慰剂组达到IGA 0/1且较基线至少下降2分的受试者比例分别为33.2%和10.8%(P<0.001),达到EASI-75的受试者比例分别为52.1%和18.1%(P<0.001)。结果显示,经过 16 周的治疗,来瑞奇珠单抗组有 38% 的患者皮肤症状清除或几乎清除(IGA 0 或 1),而安慰剂组为 12%。在症状清除或几乎清除的患者中每月一次用药,77% 的患者维持缓解达到一年。在国内,礼来于 2024 年登记了一项多中心、随机、双盲、安慰剂对照、III 期试验,旨在中至重度特应性皮炎受试者中评价来瑞奇珠单抗联合/不联合外用皮质类固醇治疗时的有效性和安全性。研究的主要终点是第 16 周达到 EASI-75 的受试者比例。具体研究结果尚未披露。目前全球仅有两款IL-13单抗获批上市,即Tralokinumab(Leo Pharm)和来瑞奇珠单抗(礼来)。
https://mp.weixin.qq.com/s/TMuqTf23nyCKb540QZpbXQ
相关News
- 从信息连接到全球商机,Drugdu.com滴度医贸网的十年 2026-06-10
- 劲方医药小分子新药获美国FDA快速通道资格,针对肺癌丨产业新闻 2026-06-08
- 每月一次!全球首款IgA肾病新药国内获批上市 2026-06-08
- 全球首个,广东药企重磅1类新药获批上市 2026-06-08
- 金赛药业自研1类新药双适应症获批临床,覆盖儿科与神经领域 2026-06-08





