合源生物第三项新药上市申请!源瑞达治疗儿童急性淋巴细胞白血病适应症新药上市申请获受理,中国原研 CAR-T为儿童患者带来突破性治疗选择
2026-05-14
来源: drugdu
 40
40

2026年5月11日,合源生物科技股份有限公司(下称 “合源生物”)宣布,国家药品监督管理局(NMPA)已正式受理其核心产品源瑞达 ®(纳基奥仑赛注射液)用于治疗儿童复发或难治性B 细胞急性淋巴细胞白血病(r/r B-ALL)的上市申请(NDA)。这是中国原研CD19 CAR-T 产品源瑞达 ®在继治疗成人复发或难治性 B 细胞急性淋巴细胞白血病以及治疗成人复发或难治性大B细胞淋巴瘤的两项新药上市申请获得国家药监局批准后提交的第三项新药上市申请,是合源生物在CAR-T细胞创新药研发上所取得的又一重大里程碑。源瑞达 ®成为唯一能够同时覆盖成人急性淋巴细胞白血病、儿童急性淋巴细胞白血病和大B细胞淋巴瘤的CAR-T产品,为更多患者带来突破性治疗选择。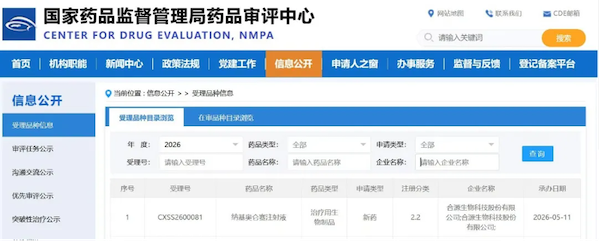 急性淋巴细胞白血病(ALL)是儿童最常见的血液恶性肿瘤,占儿童白血病的 70% 以上。尽管联合化疗与精准分层治疗已将儿童 ALL 整体生存率提升至80%-90%,但仍有20%-25% 的患者会出现复发或原发难治,这部分人群预后极差,原发难治患者再挽救有效率仅 31%,中位总生存期(OS)不足1 年。随着治疗线数增加,儿童患者的缓解率持续下降,且长期多药化疗带来的严重感染、骨髓抑制、器官毒性等副作用,严重影响患儿生存质量与长期预后,临床亟需安全、高效的创新治疗手段。
急性淋巴细胞白血病(ALL)是儿童最常见的血液恶性肿瘤,占儿童白血病的 70% 以上。尽管联合化疗与精准分层治疗已将儿童 ALL 整体生存率提升至80%-90%,但仍有20%-25% 的患者会出现复发或原发难治,这部分人群预后极差,原发难治患者再挽救有效率仅 31%,中位总生存期(OS)不足1 年。随着治疗线数增加,儿童患者的缓解率持续下降,且长期多药化疗带来的严重感染、骨髓抑制、器官毒性等副作用,严重影响患儿生存质量与长期预后,临床亟需安全、高效的创新治疗手段。
源瑞达®(纳基奥仑赛注射液)是合源生物具有完全自主知识产权的靶向 CD19 CAR-T 细胞治疗产品,拥有全球独特的 CD19 scFv(HI19a)结构与国际领先的生产工艺,在注册临床研究和真实世界中均表现出一致的优异疗效和安全性。此前,源瑞达®于2023年11月获得国家药监局批准上市用于治疗成人复发或难治性B细胞急性淋巴细胞白血病,是国内唯一用于治疗成人急淋白血病的CAR-T产品。2025年11月,源瑞达®获批第二项新药上市,用于成人复发或难治性大B细胞淋巴瘤,成为国内唯一同时覆盖白血病与淋巴瘤两大血液肿瘤的CAR-T 产品。
源瑞达®(纳基奥仑赛注射液)治疗儿童复发或难治性B细胞急性淋巴细胞白血病于2025 年8 月获得国家药监局药品审评中心(CDE)“突破性治疗药物”资格认定,享受优先审评等加速政策支持;2026 年5月11日,儿童急淋新药上市申请正式获国家药监局受理,基于其在注册临床试验中展现的优异疗效与可控安全性,有望快速获批上市。
纳基奥仑赛注射液在治疗儿童 r/r B-ALL 的关键注册临床研究(I/II 期,多中心、单臂、开放标签)数据显示:高客观缓解率(ORR):可评估患者的ORR可达90%,,其中完全缓解(CR)率超70%,显著优于传统挽救化疗;深度 MRD 阴性:所有缓解患者均达微小残留病(MRD)阴性,MRD阴性率100%,为长期无病生存奠定核心基础。快速缓解与持久获益:缓解患者均是在细胞回输后28 天首次评估时达到MRD 阴性缓解,部分患儿已获得超过2 年的持续无病生存,回归正常生活与学习。不良反应以1-2 级细胞因子释放综合征(CRS)为主,≥3级 CRS 发生率低,无治疗相关死亡;免疫效应细胞相关神经毒性综合征(ICANS)发生率低且经临床处理后均恢复无后遗症,整体安全性与成人患者一致,符合儿童治疗耐受性要求。
关于合源生物
合源生物创立于2018年6月,已成长为中国细胞药物产业自主创新的引领者,致力于成为全球领先的细胞与基因创新技术驱动的新一代生物医药企业。公司首个核心产品源瑞达®(纳基奥仑赛注射液,CNCT19)于2023年11月正式获国家药品监督管理局批准上市。该产品是中国白血病治疗领域首个CAR-T药物,也是中国全自主创新的首个CD19 CAR-T药物。公司深度合作国家一流院所,构建了以CAR技术平台、基因编辑技术平台等为核心的国际化新药研发体系,拥有覆盖血液肿瘤、实体肿瘤及自身免疫性疾病等疾病领域的10余种管线产品在研。
https://mp.weixin.qq.com/s/Fg8qXR2YzFIRgXJIgIrvrw
责编: editor相关News
- 新华制药取得止咳平喘药品氨溴特罗口服溶液药品注册证书 2026-05-14
- 刚刚,百济神州重磅新药在美国获批上市! 2026-05-14
- 【企业推荐】天津市凯峰科技有限公司 2026-05-14
- 恒瑞医药双箭齐发!HER3 ADC领跑者SHR-A2009再获IND,阿得贝利单抗进军KRAS突变实体瘤 2026-05-14
- 伊米诺康完成2.5亿元A轮融资,加速打造全球领先的全人源抗体发现平台 2026-05-14
您已成功订阅,无需重复提交。
确认
邮件订阅
请输入正确邮箱!
订阅
邮件订阅热门医贸资讯,了解第一手信息。
行业动态更多
-
新华制药取得止咳平喘药品氨溴特罗口服溶液药品注册证书
2026-05-14 -
刚刚,百济神州重磅新药在美国获批上市!
2026-05-14 -
【企业推荐】天津市凯峰科技有限公司
2026-05-14





